Em nossas vidas diárias, além da luz solar quente, Luzes LED se tornaram a principal fonte de iluminação. Desde as telas dos celulares que nos acompanham em todos os momentos até a aconchegante e confortável iluminação da casa, e depois para as deslumbrantes luzes de néon que adornam as cidades à noite, As luzes LED cativam as pessoas com seu charme único. Então, por que exatamente as luzes LED podem emitir luz, e como eles são capazes de exibir uma variedade tão rica de cores como o branco, verde, azul, e vermelho? Que mistérios científicos estão por trás deste fenômeno? Vamos nos aprofundar e explorar juntos.
Por que os LEDs podem emitir luz?
Um LED é na verdade um diodo emissor de luz, que é feito de materiais semicondutores. O princípio por trás da capacidade de um LED de emitir luz é baseado em sua estrutura única de banda de energia e no processo de recombinação de portadores..
Os materiais semicondutores são cristais de alta qualidade nos quais os átomos estão dispostos periodicamente no espaço.. Cada átomo consiste em um núcleo carregado positivamente e elétrons carregados negativamente. Como um cristal contém um grande número de átomos, esses átomos interagem entre si. Esta interação periódica forma bandas de energia dentro do cristal, e existem inúmeras bandas de energia presentes. Cada banda de energia fornece muitas posições para os elétrons ocuparem, e a distribuição de elétrons dentro de uma banda de energia progride das posições de energia mais baixa para aquelas com energia mais alta.

Dentro das faixas de energia de um cristal, alguns são ocupados por elétrons, enquanto outros não são. Entre as faixas de energia ocupadas, aquele com maior energia, se apenas parcialmente preenchido com elétrons, é conhecida como banda de condução. Os elétrons na banda de condução residem em níveis de energia relativamente altos e possuem energia suficiente para se moverem livremente., formando assim uma corrente elétrica. Por outro lado, se esta banda de energia estiver completamente preenchida com elétrons, é chamada de banda de valência. Os elétrons na banda de valência estão em níveis de energia mais baixos, e sua energia é insuficiente para permitir que se movam livremente. Existe uma certa lacuna de energia entre o topo da banda de valência e o fundo da banda de condução, conhecido como bandgap ou banda proibida. Os elétrons não podem residir nesta região, embora eles possam atravessá-lo.
Quando uma tensão externa é aplicada, alguns elétrons na banda de valência podem ser excitados para a banda de condução, formando portadores de carga que se movem livremente. Enquanto isso, na banda de valência originalmente totalmente ocupada, a ausência de alguns elétrons deixa posições vagas, que chamamos de buracos. Os processos de movimento e recombinação destes portadores de carga dentro do material semicondutor são cruciais para alcançar a emissão de luz.
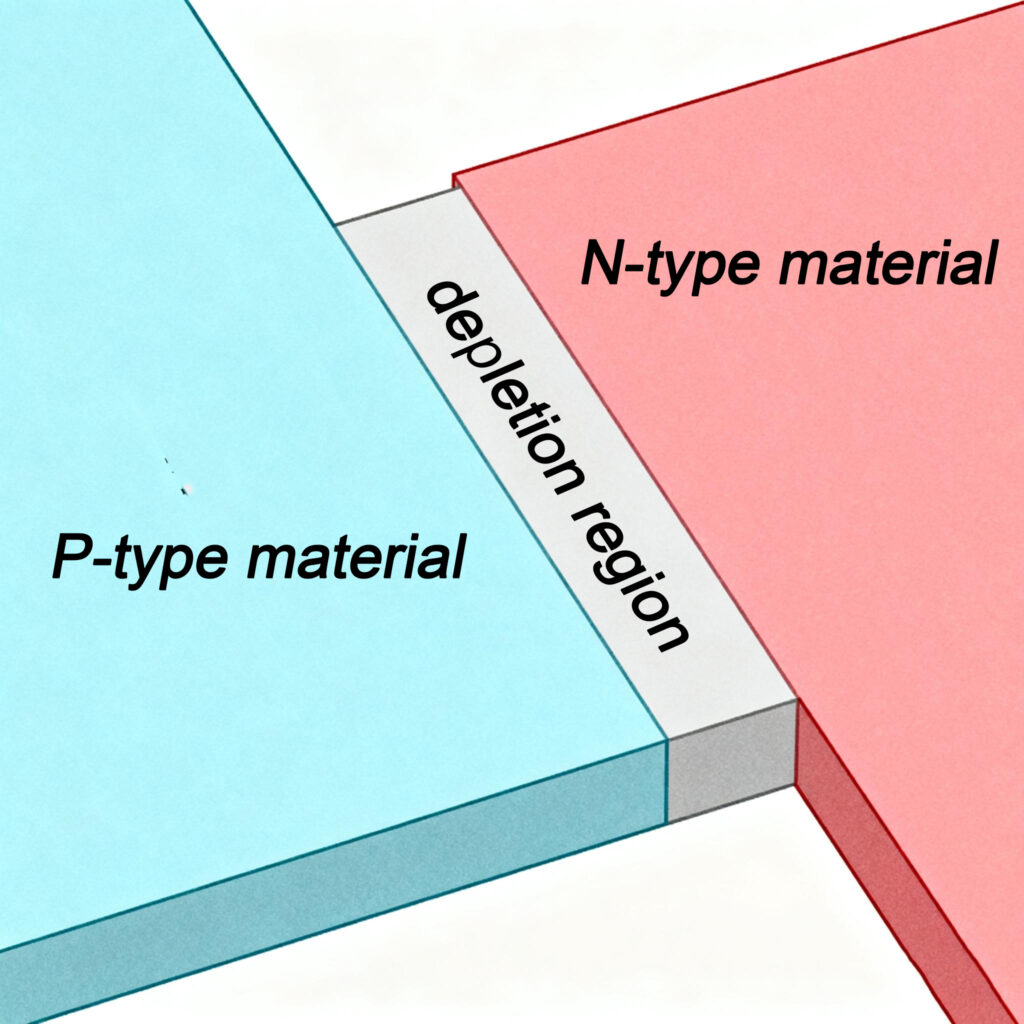
Um LED é um diodo emissor de luz, que consiste em uma estrutura de diodo com uma junção PN formada pela combinação de semicondutores tipo P e tipo N. Quando colocamos os semicondutores tipo P e tipo N juntos, mesmo sem conectá-los a um circuito, alguns elétrons se difundirão do semicondutor tipo N para o semicondutor tipo P e cairão nos buracos do material tipo P. Isso faz com que o semicondutor tipo P adquira uma leve carga negativa, enquanto o semicondutor do tipo N torna-se ligeiramente carregado positivamente, resultando na formação de um campo elétrico interno, conhecida como junção PN. Dentro da junção PN, quando os elétrons encontram buracos, elétrons na banda de condução irão saltar para as lacunas na banda de valência. Durante este processo de recombinação elétron-buraco, a energia é liberada na forma de luz. Este é o princípio fundamental por trás de como os LEDs emitem luz.
Luzes LED emitem luz de cores diferentes
O nível de energia envolvido no processo de emissão de luz está relacionado à estrutura da banda de energia do material semicondutor. Diferentes materiais e estruturas de bandas de energia resultam em diferentes comprimentos de onda e cores de emissão. Especificamente:
Transição de elétrons e diferença de energia
Quando um elétron transita de um orbital de maior energia para um orbital de menor energia, libera energia que se propaga na forma de ondas eletromagnéticas. A diferença de energia liberada durante as transições eletrônicas varia entre os diferentes elementos, correspondendo à luz de diferentes comprimentos de onda. Quanto maior a energia, quanto menor o comprimento de onda. No espectro, a energia necessária aumenta da esquerda para a direita. É por isso que os LEDs vermelhos foram inventados primeiro, pois requerem a menor quantidade de energia, seguido de verde, e depois azul. É também por isso que a invenção dos LEDs azuis foi um desafio, como a luz azul requer mais energia.
Comprimentos de onda de 400-500 nanômetros correspondem à luz azul, 500-600 nanômetros para luz verde, e 600-700 nanômetros para luz vermelha.
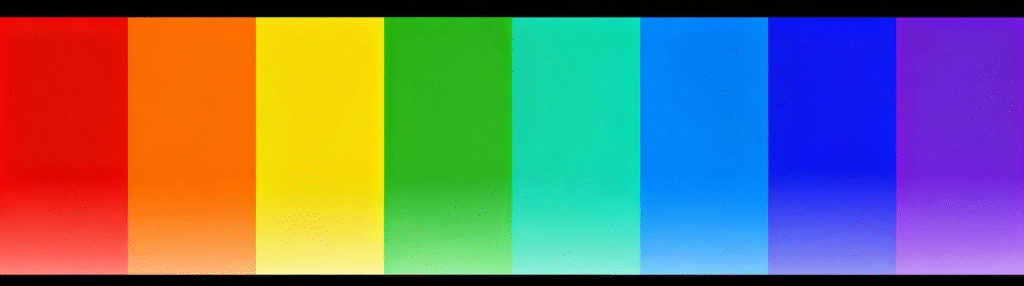
Seleção de materiais e controle de cores
A junção PN dentro de um LED é geralmente composta de compostos como fosfeto de arsenieto de gálio. Quando diferentes materiais são usados, os comprimentos de onda da luz emitida após a eletrificação variam. Portanto, simplesmente alterando o material da junção PN interna, diodos emissores de luz de cores diferentes podem ser produzidos.
LED azul: Quando o nitreto de gálio é usado como material semicondutor, a energia de transição do elétron é relativamente alta, liberando luz com comprimento de onda de aproximadamente 460 nanômetros, que parece azul. Este é o princípio por trás da emissão de LEDs azuis.
LED verde: Quando o fosfeto de gálio é utilizado, a luz emitida tem um comprimento de onda de cerca de 560 nanômetros, apresentando uma cor verde. Isso explica o mecanismo de emissão dos LEDs verdes.
LED vermelho: Arsenieto de gálio, por outro lado, emite luz com um comprimento de onda de aproximadamente 660 nanômetros, aparecendo vermelho. Este é o princípio subjacente à emissão de LEDs vermelhos.
Para produzir luz branca com LEDs, também conhecidos como LEDs brancos, projetos adicionais são necessários. Um método envolve a combinação de diodos emissores de luz de cores diferentes para criar um efeito de luz branca.. Outra abordagem utiliza um LED azul revestido com fósforo. A luz azul emitida pelo LED ilumina o fósforo, convertendo uma parte da luz azul em outras cores de luz. O efeito final aparece como luz branca.
Através da introdução detalhada acima sobre o princípio de emissão de luz dos LEDs e os mecanismos por trás de sua emissão de cores diferentes, Acredito que todos agora têm uma compreensão mais profunda dos LEDs. Com avanços tecnológicos contínuos, as aplicações dos LEDs em vários campos, como iluminação e displays, tornar-se-ão ainda mais difundidas e notáveis.